پاسخ سیستم ایمنی در برابر قارچها
نوتروفیلها و ائوزینوفیلها
نوتروفیلها سلولهای اجرائی اولیه در التهاب حاد هستند که به تعداد زیاد در جریان گردش خون حضور داشته و بهوسیلهی یک سری از حوادثی که بهدقت تنظیم میشود، از طریق چسبیدن به اندوتلیوم عروق و مهاجرت از عرض اندوتلیوم و از میان بافت، خود را بهسرعت به محل عفونت میرسانند. محصولات میکروبی، اجزاء کمپلمان (بهویژه C۵a)، کموکاینها (بهویژه IL-۸) و متابولیتهای اسید آراشیدونیک بر روی سلولهای اندوتلیال و نوتروفیلها عمل میکنند تا این سری حوادث را آغاز کنند. در محل التهاب، اتصال به میکروبها توسط رسپتورهای اختصاصی نوتروفیلها واقع میشود و اگر میکروب توسط C۳ یا IgG اپسونیزه شده باشد این عمل تسهیل میگردد. ممکن است در غیاب اپسونینها به علت حضور لیگاندها بر روی سطوح میکروبی (مانند مانوز و بتاگلوکان) که توسط رسپتورهای نوتروفیلی مورد شناسائی قرار میگیرند، اتصال رخ دهد. بعد از اتصال، معمولاً فاگوسیتوز واقعی (اینترنالیزاسیون) ارگانیسم اتفاق میافتد. فرآیند کشتن میکروارگانیسمها میتواند در اثر مکانیزمهای اکسیداتیو یا غیراکسیداتیو رخ دهد. مکانیزمهای اکسیداتیو به فرآیندهایی برمیگردد که وابسته به انفجار تنفسی است که بهموجب آن اکسیژن ملکولی به آنیون سوپراکساید احیاء میگردد. مقدار عمدهی این آنیون سوپراکساید به پراکسید هیدروژن تبدیل میشود. پراکسید هیدروژن فعالیت ضدمیکروبی ضعیفی دارد. هرچند که در یک واکنش که بهوسیلهی آنزیم میلوپراکسیداز نوتروفیلی کاتالیز میشود پراکسید هیدروژن میتواند با یک یون هالید وارد واکنش شده و اکسیدانتها را با فعالیت قوی ضدمیکروبی تشکیل دهد (مثال: اسید هیپوکلرو). منوسیتها و ماکروفاژها نیز در اثر تحریک میتوانند انفجار تنفسی را- اگرچه در یک سطح فعالیتی که بهطور قابلتوجهی کمتر از نوتروفیلها است- به راه بیاندازند، علاوه بر این ماکروفاژهای بالغ فاقد میلوپراکسیداز هستند. گرانولهای نوتروفیلها حاوی موادی هستند که میتوانند فعالیت میکروبکشی غیروابسته به اکسیژن را واسطه کنند و اینها شامل دفنسینها، لاکتوفرین و کلپروتکتین میباشد. در طول فعال شدن نوتروفیل، گرانولها تخلیه شده و محتوای خود را به داخل فاگولیزوزوم و فضای خارج سلولی آزاد میکنند.
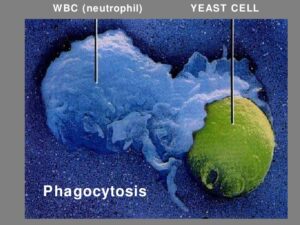
نوتروفیلها و ائوزینوفیلها
از منظر بالینی یک ارتباط قوی بین نوتروپنی با کاندیدیازیس منتشره و آسپرجیلوزیس تهاجمی وجود دارد. بدون شک این ارتباط نهتنها از اهمیت ویژهی نوتروفیلها در دفاع میزبان علیه این دو میکوز حکایت میکند، بلکه همچنین مربوط به فراوانی میزان برخورد با این قارچهای همهجا حاضر نیز میباشد. بسیاری از میکوزهای دیگر شامل زیگومیکوز، فوزاریوز و سودوآلشریازیس اگرچه هنوز نسبتاً نادر هستند، با این وجود با شیوع روزافزونی در میزبانان نوتروپنیک دیده میشوند. ارتباط نوتروپنی با میکوزها موجب شده تا تحقیقات زیادی بر روی واکنشهای بین نوتروفیلها با تعداد متنوعی از قارچها بهویژه کاندیدا و آسپرجیلوس صورت گیرد. در شرایط آزمایشگاهی نوتروفیلهای انسان میتوانند سلولهای مخمری، سودوهایفی و هایفی کاندیدا آلبیکنس و نیز هایفی آسپرجیلوس فومیگاتوس را بکشند. در مقابل، کنیدیهای آسپرجیلوس فومیگاتوس که فرم استنشاق شدهی ارگانیسم هستند علیرغم اینکه به سهولت فاگوسیت میشوند، نسبت به کشته شدن توسط نوتروفیلها مقاوم هستند. سلولهای هایفی کاندیدا و آسپرجیلوس آنقدر بزرگ هستند که نتوانند توسط نوتروفیلها بلعیده شوند، اگرچه گروهی از نوتروفیلها میتوانند به سطح قارچی چسبیده و آن را بکشند. هایفی هر دو قارچ نوتروفیلها را تحریک میکنند تا فرآیند انفجار تنفسی و دگرانولاسیون راه افتد. اکسیدانتهای ایجادشده (بهعنوان مثال پراکسید هیدروژن و اسید هیپوکلرو) و تولیدات گرانولی که آزاد میشوند (مانند دفنزینها) خواص قارچکشی دارند. اهمیت نوتروفیلها در دفاع علیه کاندیدا آلبیکنس و آسپرجیلوس فومیگاتوس و سایر قارچهای کاتالاز مثبت با کثرت این میکوزها (در یک سری بزرگ به میزان ۲۰ درصد) در بیماری گرانولوماتوز مزمن، CGD (یک اختلال ارثی مربوط به NADPH oxidase) برجستهتر میشود. نوتروفیلهای مربوط به این دسته از بیماران در توانائی خود برای به راه انداختن انفجار تنفسی دچار نقص هستند و تنها مقادیر ناکافی و اندکی اکسیدانتهای میکروبکش تولید میکنند. به دنبال این مسئله نوتروفیلهای بیماران CGD در کشتن ارگانیسمهای کاتالاز مثبت که شامل گونههای آسپرجیلوس و کاندیدا هستند، مشکل دارند. در مورد ارگانیسمهای کاتالاز منفی، نوتروفیلهای بیماران CGD قادر هستند نقص پراکسید هیدروژن را با استفاده از پراکسید هیدروژنی که توسط میکروارگانیسمها تولید شدهاند، تأمین نمایند. ارگانیسمهای کاتالاز مثبت با تجزیهی پراکسید هیدروژنی که تولید میکنند فاگوسیت را از پراکسید هیدروژن درونزاد خود محروم میکنند.
نوتروفیلها دارای رسپتورهای سایتوکاین هستند و تحریک نوتروفیلها با سایتوکاینهای مناسب میتواند موجب افزایش قدرت قارچکشی آنها شود که مطرحکنندهی مکانیزمهای فیدبکی است که به آن وسیله سلولهای تکهستهای تحریک شده، سایتوکاینها را تولید میکنند که در عوض نوتروفیلها را برای عمل قارچکشی مؤثرتر فعال میکنند. استعمال درون بدنی in vivo اینترفرون گامای نوترکیب به بیماران CGD نشان میدهد که بهصورت قابلتوجهی انسیدانس عفونتهای وخیم کاهش مییابد. نوتروفیلهای بهدستآمده از بیماران CGD که با اینترفرون گاما درمان شدهاند ظرفیت آسیب رساندن به هایفی آسپرجیلوس فومیگاتوس را کسب میکنند. برعکس، فعالیت کاندیداکشی نوتروفیلها بهوسیلهی سایتوکاینهای ضدالتهابی IL-۴ و IL-۱۰ دچار اختلال میشود. پروسهای که ممکن است آسیبی را که بهوسیلهی پاسخ التهابی فراوان و پرشاخ و برگ ایجاد شود را محدود نماید. نوتروفیلها در اثر تحریک بهوسیلهی کاندیدا آلبیکنس و آسپرجیلوس فومیگاتوس سایتوکاینهای پیشالتهابی و ضدالتهابی، هر دو را ترشح میکنند. پاتولوژی کاندیدیازیس و آسپرجیلوزیس منتشره تهاجم عروقی است، این یافته موجب مطالعهی واکنش بین کاندیدا آلبیکنس و آسپرجیلوس فومیگاتوس با اندوتلیوم عروق شده و اینکه نوتروفیلها چگونه این واکنش را تحت تأثیر قرار میدهند. مولکولهای چسبنده (adhesins) متعددی شرح داده شدهاند که این پروسه را تسهیل میکنند که شامل آنالوگهای اینتگرین (پروتئینهای قارچی که مشابهت آنتیژنیک و عملکردی با اینتگرینهای پستانداران نشان میدهند) هستند که لیگاندهای اینتگرین را بر روی سلولهای اندوتلیال شناسائی میکنند. بسیاری از این رسپتورهای همانند هم، احتمالاً چسبیدن کاندیدا آلبیکنس به سلولهای اپیتلیال را وساطت میکنند.
در مقایسه با نوتروفیلها، اطلاعات کمتری در مورد سهم ائوزینوفیلها در پاسخهای میزبان در برابر قارچهای مهاجم وجود دارد. ائوزینوفیلها عموماً در ارتباط با بیماریهای آلرژیک قارچی که عمدتاً شامل سینوزیت و آسم است، دیده میشوند. در چنین مواردی ائوزینوفیلها به علت آزادسازی محصولات سمی از خودشان که شامل پراکسیداز ائوزینوفیلی و پروتئین بازی مهم آن است، اثرات زیانبخشی را از خود بر جای میگذارند. در شرایط آزمایشگاهی (in vitro) مواد استخراجشده از قارچهای محیطی آلترناریا آلترناتا و پنیسیلیوم نوتاتوم موجب القاء اگزوسیتوز ائوزینوفیلها در افراد نرمال میشود. یک پاسخ ائوزینوفیلیک گاهی اوقات در انسانها در ارتباط با برخی از میکوزها بهویژه در کوکسیدیوئیدومایکوزیس دیده میشود.
فاگوسیتهای تکهستهای
فاگوسیتهای تکهستهای نسبت به بروز یک پاسخ ایمنی محافظتی به تعدادی از مهمترین پاتوژنهای قارچی نقش مرکزی دارند. منوسیتها، ماکروفاژهای مقیم بافتی و سلولهای دندریتیک بخشی از خط مقدم ایمنی ذاتی با واسطهی سلولی را تشکیل میدهند، علاوه بر این فاگوسیتهای تکهستهای بهویژه سلولهای دندریتیک در برقراری ارتباط بین پاسخهای ایمنی ذاتی و تطبیقی بهوسیلهی به راه انداختن و ترویج پاسخهای ایمنی با واسطهی سلول T اختصاصی نقش بسیار مهمی دارند. سلولهای T فعالشده میتوانند سایتوکاینها را ترشح کنند و این سایتوکاینها فاگوسیتها را فعال میکنند تا بهصورت سلولهای اجرائی بسیار قویتری درآیند. به نظر میرسد که بسیاری از قارچها بهویژه کریپتوکوکوس نئوفرمنس و هیستوپلاسما کپسولاتوم با بقاء درون فاگوسیتها خود را تطبیق میدهند. (شکل ۱)
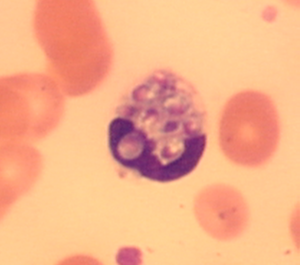
شکل شماره ۱: تصویر هیستوپلاسما کپسولاتوم درون یک منوسیت در خون محیطی. گسترش خون محیطی که از یک بیمار ایدزی و مبتلا به هیستوپلاسموز منتشرهی پیشرونده تهیه شده است. سلولهای مخمری هیستوپلاسما کپسولاتوم درون سلول منوسیت دیده میشوند.
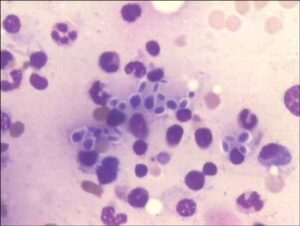
شکل شماره ۲: سلولهای مخمری هیستوپلاسما کپسولاتوم در نمونهی آسپیرهی مغز استخوان، هالهی شفاف اطراف مخمرها قابلتوجه است.
سلولهای دندریتیک
سلولهای دندریتیک در تمام ارگانهای بدن حضور دارند و بهعنوان نگهبان عمل میکنند. سلولهای دندریتیک هنگام مواجهه با آنتیژنها و یک سیگنال بالغ شدن به بافت لنفاتیک مهاجرت میکنند و در آنجا بالغ میشوند، سایتوکاینها را ترشح میکنند و پاسخهای ایمنی با واسطهی سلولی را شروع میکنند. واکنش سلولهای دندریتیک با سلولهای T در عقدههای لنفاوی نهتنها منجر به زایش و توسعه و گسترش سلولهای T اختصاصی نسبت به آنتیژن میگردد، بلکه همچنین موجب پولاریزه شدن سلولهای T به متمایز شدن به سلولهای T رگولاتوری یا Th۱ و Th۲ میشوند. همچنین دندریتیک سلها پلهای کلیدی بین ایمنی تطبیقی و ایمنی ذاتی هستند و بنابراین تعجبآور نیست که در مطالعات متنوعی نشان داده شده است که سلولهای دندریتیک در به راه انداختن پاسخهای سلولهای +CD۴ و +CD۸ علیه پاتوژنهای قارچی اهمیت اساسی دارند، هرچند که تصور میشود عمل اولیهی آنها آغاز کردن پاسخهای ایمنی تطبیقی از طریق فرآیند بیان آنتیژن است. سلولهای دندریتیک همچنین سلولهای اجرائی فاگوسیتیک هستند. پاتوژنهای قارچی که توسط سلولهای دندریتیک فاگوسیت شده یا علیه آنها فعالیت ضدقارچی انجام میشود شامل کاندیدا آلبیکنس، هیستوپلاسما کپسولاتوم، آسپرجیلوس فومیگاتوس، کریپتوکوکوس نئوفرمنس و کوکسیدیوئیدس پوساداسی میباشند. سلولهای دندریتیک برای فاگوسیتوز سلولهای کریپتوکوکوس نئوفرمنس کپسولدار نیاز به اپسونیزاسیون با کمپلمان یا آنتیبادی دارند، درحالیکه برای سایر قارچها لیگاندهائی که بر روی سطوح قارچی حضور دارند بهوسیلهی رسپتورهای سلولهای دندریتیک مورد شناسائی قرار میگیرند. مکانیزمهائی که بهوسیلهی آن سلولهای دندریتیک پاتوژنهای قارچی را میکشند بهخوبی مشخص نشده است، هرچند که در یک مطالعه از شرکت داشتن هیدرولازهای لیزوزومال نام برده شده است. سلول دندریتیک میتواند به دنبال فاگوسیتوز بالغ شود، سایتوکاینها را ترشح کند و آنتیژنهای قارچی را بیان کند. مرفوتایپ قارچ میتواند طبیعت پاسخ ایمنی را تحت تأثیر قرار دهد. فاگوسیتوز سلولهای مخمری و کنیدیهای آسپرجیلوس فومیگاتوس توسط سلولهای دندریتیک منجر به پاسخ سلولی نوع Th۱ میشود، درحالیکه فرمهای هایفی این قارچها سلولهای دندریتیک را تحریک میکنند تا پاسخ سلولی نوع Th۲ را القاء نمایند.
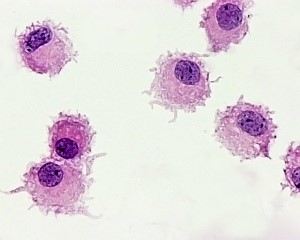
شکل شماره ۳: نمایی از سلولهای دندریتیک
ماکروفاژها
ماکروفاژها از منوسیتهای در گردش به دنبال بکارگیری در بافت و تمایز بعدی آنها منشأ میگیرند. خواص ضدقارچی ماکروفاژها به مقدار زیادی تحت تأثیر محل آناتومیک است که در آن تمایز صورت میگیرد و همچنین تحت تأثیر حالت فعالسازی ماکروفاژ است. فعالسازی ماکروفاژها بهوسیلهی سایتوکاینهای مشتقشده از لنفوسیتها بهویژه اینترفرون گاما ممکن است خواص قارچکشی این فاگوسیتها را آشکار کند. این مسئله احتمالاً بیانگر اهمیت حیاتی ایمنی با واسطهی سلولی در کنترل بسیاری از قارچهای پاتوژن است. بهاستثنای کاندیدا آلبیکنس، برای اکثر قارچهایی که بیماری سیستمیک ایجاد میکنند، مواجههی ابتدائی بهوسیلهی استنشاق سلولهای قارچی هوابرد ایجاد میشود، بنابراین ماکروفاژهای برونکوآلوئلار بهویژه یک جزء مهم از دفاع میزبان را تشکیل میدهند. ماکروفاژهای برونکوآلوئلار رشد تعدادی از قارچها را مهار میکنند و معمولاً فعالیت ضدقارچی بزرگتری نسبت به سایر جمعیــــتهای ماکروفاژی دارند. در شرایط آزمایشگاهی (in vitro) ماکروفاژهای برونکوآلوئلار میتوانند کنیدیهای آسپرجیلوس فومیگاتوس را بکشند ولی روی هایفی این قارچ اثری ندارند. برعکس، نوتروفیلها بر روی کنیدی اثرات مرگآوری ندارند ولی میتوانند هایفی را بکشند. در شرایط داخل بدن این دو نوع دفاع فاگوسیتی در ترکیب با یکدیگر عمل میکنند تا از استقرار عفونت جلوگیری کنند. کنیدیهائی که از کشته شدن توسط ماکروفاژهای برونکوآلوئلار مقیم بافتی فرار میکنند و ژرمیناسیون پیدا میکنند نسبت به حمله توسط نوتروفیلها حساس خواهند بود. ماکروفاژهای برونکوآلوئلار علیه دیگر گونههای قارچی از قبیل کریپتوکوکوس نئوفرمنس، رایزوپوس آریزوس و بلاستومایسس درماتیتیدیس فعالیت دارند. در مقابل، میکروکونیدی هیستوپلاسما کپسولاتوم یعنی فرم استنشاقشدهی ارگانیسم، به دنبال بلعیده شدن توسط ماکروفاژهای برونکوآلوئلار روند تغییر فاز را به سمت سلولهای مخمری انجام داده و سپس تکثیر مییابد.
همانند نوتروفیلها، منوسیتها و ماکروفاژها فعالیت ضدقارچی خود را بهوسیلهی مکانیزمهای اکسیداتیو و غیراکسیداتیو اعمال میکنند. میانجیهای واکنشپذیر نیتروژن شامل اکسید نیتریک که توسط ماکروفاژهای فعالشده تولید میشوند یک نقش کلیدی در عمل ضدقارچی ماکروفاژهای موشی دارند، هرچند به علت کمتر ساخته شدن میانجیهای واکنشپذیر نیتروژن بهوسیلهی ماکروفاژهای انسانی از کاربرد این مکانیزم ضدقارچی در سلولهای انسانی اطمینانی حاصل نیست. فعالیت ضدقارچی واسطههای غیراکسیداتیو کمتر مشخص شدهاند اما احتمالاً شامل آنزیمهای تجزیهکننده و پپتیدهای ضدمیکروبی هستند. آنزیمها شامل لکتینازها که نقش مهمی در تجزیه و تلاشی دیوارهی سلول قارچی بازی میکنند، بهخوبی شرح داده شدهاند. به نظر میرسد که اسیدیفیکاسیون فاگوزوم بدنبال جوش خوردن فاگوزوم– لیزوزوم تا حدودی و به درجاتی رخ دهد اما ممکن است بسان یک شمشیر دو لبه عمل نماید.
یک pH پائین فعالیت مطلوب هیدرولازهای لیزوزومال را تشویق میکند و نیز آهن را برای قارچ قابل دسترسی مینماید. هیستوپلاسما کپسولاتوم مکانیزمهائی را ایجاد میکند که بهوسیلهی آن میتواند pH فاگوزومال را در حدود ۵/۶ نگاه دارد و بنابراین به ارگانیسم اجازه میدهد که آهن را بدست آورد و فعالیت هیدرولازهای لیزوزومال ماکروفاژ را به حداقل برساند. عواملی مثل کلروکین که pH فاگولیزوزومال را بالا میبرد بهصورت قابلتوجهی فعالیت ضدقارچی ماکروفاژهای انسانی را در برابر هیستوپلاسما کپسولاتوم و کریپتوکوکوس نئوفرمنس افزایش میدهد. در مورد هیستوپلاسما کپسولاتوم، کلروکین با فراهم کردن محدودیت آهن در pH بالاتر و در مورد کریپتوکوکوس نئوفرمنس اثر کلروکین مستقل از فقدان آهن بوده و به رشد ضعیف این قارچ در pH بالاتر ارتباط دارد.