چگونه احساسات را درک میکنیم؟
توانایی ما برای احساس گرما، سرما و لمس برای بقا ضروری است و بر تعامل ما با جهان پیرامون تأکید میکند. در زندگی روزمره ما این احساسات را بدیهی میدانیم، اما چگونه تکانههای عصبی آغاز میشوند تا دما و فشار درک شوند؟ این سؤال توسط برندگان امسال جایزه نوبل پزشکی و فیزیولوژی حل شده است. دیوید جولیوس از کپسایسین، ترکیبی تند از فلفل چیلی که باعث سوزش میشود، برای شناسایی حسگر در انتهای عصبی پوست که به گرما واکنش نشان میدهد، استفاده کرد. اردم پاتاپوتیان از سلولهای حساس به فشار برای کشف کلاس جدیدی از حسگرها استفاده کرد که به محرکهای مکانیکی پوست و اندامهای داخلی پاسخ میدهند. این اکتشافات موفقیتآمیز، فعالیتهای تحقیقاتی نوینی را آغاز کرد که منجر به افزایش سریع درک ما از چگونگی حساسیت سیستم عصبی به گرما، سرما و محرکهای مکانیکی شد. برندگان جایزه نوبل پزشکی ۲۰۲۱ در درک ما از تعامل پیچیده بین حواس و محیط ما، حلقههای حیاتی مفقودشده را شناسایی کردند.
کپسایسین یا کاپسِیسین (Capsaicin) ماده شیمیایی تُند موجود در فلفلهای چیلی است که گیاهانی از رده کپسیکوم هستند. این ماده در فلفل های تند (سبز و قرمز) یافت میشود. علت اصلی تُند بودن فلفلها همین ماده است و خوردن آن باعث افزایش دمای بدن و احساس گرمی میشود.
جهان را چگونه درک میکنیم؟
یکی از اسرار بزرگ پیش روی بشریت این است که چگونه محیط خود را حس میکنیم. مکانیسمهای زیرین حواس ما هزاران سال است که کنجکاوی ما را برانگیخته است؛ به عنوان مثال، چگونه نور توسط چشمها تشخیص داده میشود، چگونه امواج صوتی بر گوشهای داخلی ما تأثیر میگذارند و چگونه ترکیبات شیمیایی مختلف با گیرندههای بینی و دهان ما بو و طعم ایجاد میکنند. ما همچنین راههای دیگری برای درک جهان پیرامون خود داریم؛ تصور کنید در یک روز گرم تابستان با پای برهنه از چمنزار عبور میکنید. شما میتوانید گرمای خورشید، نوازش باد و تیغههای چمن را در زیر پای خود احساس کنید. این تأثیرات دما، لمس و حرکت برای سازگاری ما با محیط در حال تغییر دائمی ضروری است. در قرن هفدهم، فیلسوفی به نام رنه دکارت، رشتههایی را تصور کرد که قسمتهای مختلف پوست را به مغز متصل میکند. به این ترتیب، اگر پای یک انسان شعله آتش را لمس کند، یک سیگنال مکانیکی به مغز او فرستاده میشود (شکل ۱). اکتشافات بعد، وجود نورونهای حسی تخصصی را نشان دادند که تغییرات محیط ما را ثبت میکنند. جوزف ارلانگر و هربرت گاسر در سال ۱۹۴۴ جایزه نوبل فیزیولوژی و پزشکی را به دلیل کشف انواع مختلف فیبرهای عصبی حسی که در لمس دردناک و غیر دردناک واکنش نشان میدهند، دریافت کردند. از آن زمان به بعد، نشان داده شده است که سلولهای عصبی برای تشخیص و انتقال انواع مختلف محرکها بسیار تخصصی هستند و به درک ظریفی از محیط اطراف خود اجازه میدهند؛ به عنوان مثال، ظرفیت ما برای احساس تفاوت در بافت سطوح از طریق نوک انگشتانمان، یا توانایی ما در تشخیص گرمای دلپذیر و گرمای دردناک.
قبل از کشفیات دیوید جولیوس و اردم پاتاپوتیان، درک ما از چگونگی حس و تفسیر سیستم عصبی محیطی هنوز حاوی یک سؤال اساسی حل نشده بود: چگونه دما و محرکهای مکانیکی در سیستم عصبی به تکانههای الکتریکی در مغز تبدیل میشوند؟

شکل ۱ تصویری را نشان میدهد که رنه دکارت فیلسوف تصور میکند که چگونه گرما سیگنالهای مکانیکی را به مغز میفرستد
در اواخر دهه 1990، دیوید جولیوس در دانشگاه کالیفرنیا با تجزیه و تحلیل چگونگی ترکیب شیمیایی کپسایسین که باعث احساس سوزش هنگام تماس با فلفل چیلی میشود، پیشرفتهای بزرگی را مشاهده کرد. تحقیقات قبلی مشخص کرده بودند که کپسایسین در سلولهای عصبی باعث ایجاد احساس درد میشوند، اما نحوه عملکرد این ماده شیمیایی مغز (نورونهای حسی عصبی) در واقع یک معمای حل نشده بود. جولیوس و همکارانش کتابخانهای از میلیونها قطعه DNA متناظر با ژنها ایجاد کردند که در نورونهای حسی بیان شده و میتوانند به درد، حرارت و لمس واکنش نشان دهند. جولیوس و همکارانش فرض کردند که کتابخانه شامل یک قطعه DNA است که پروتئین را قادر به واکنش نسبت به کپسایسین میکند. آنها ژنهای فردی از این مجموعه را در سلولهای کشتشده بیان کردند که معمولاً به کپسایسین واکنش نشان نمیدهند. پس از جستجوی پرزحمت، یک ژن منفرد شناسایی شد که قادر بود سلولها را به کپسایسین حساس کند (شکل 2)؛ بنابراین ژن سنجش کپسایسین پیدا شد! آزمایشهای بیشتر نشان داد که ژن شناسایی شده، یک پروتئین کانال یونی جدید را رمزگذاری میکند و این گیرنده کپسایسین تازه کشفشده بعداً TRPV1 نامگذاری شد که در بازوی کوتاه کروموزوم شماره 17 بهصورت 17p13.2 مستقر است. وقتی جولیوس توانایی پروتئین در پاسخ به گرما را بررسی کرد، متوجه شد که یک گیرنده حسگر را کشف کرده است که در دماهای دردناک فعال میشود (شکل 2).
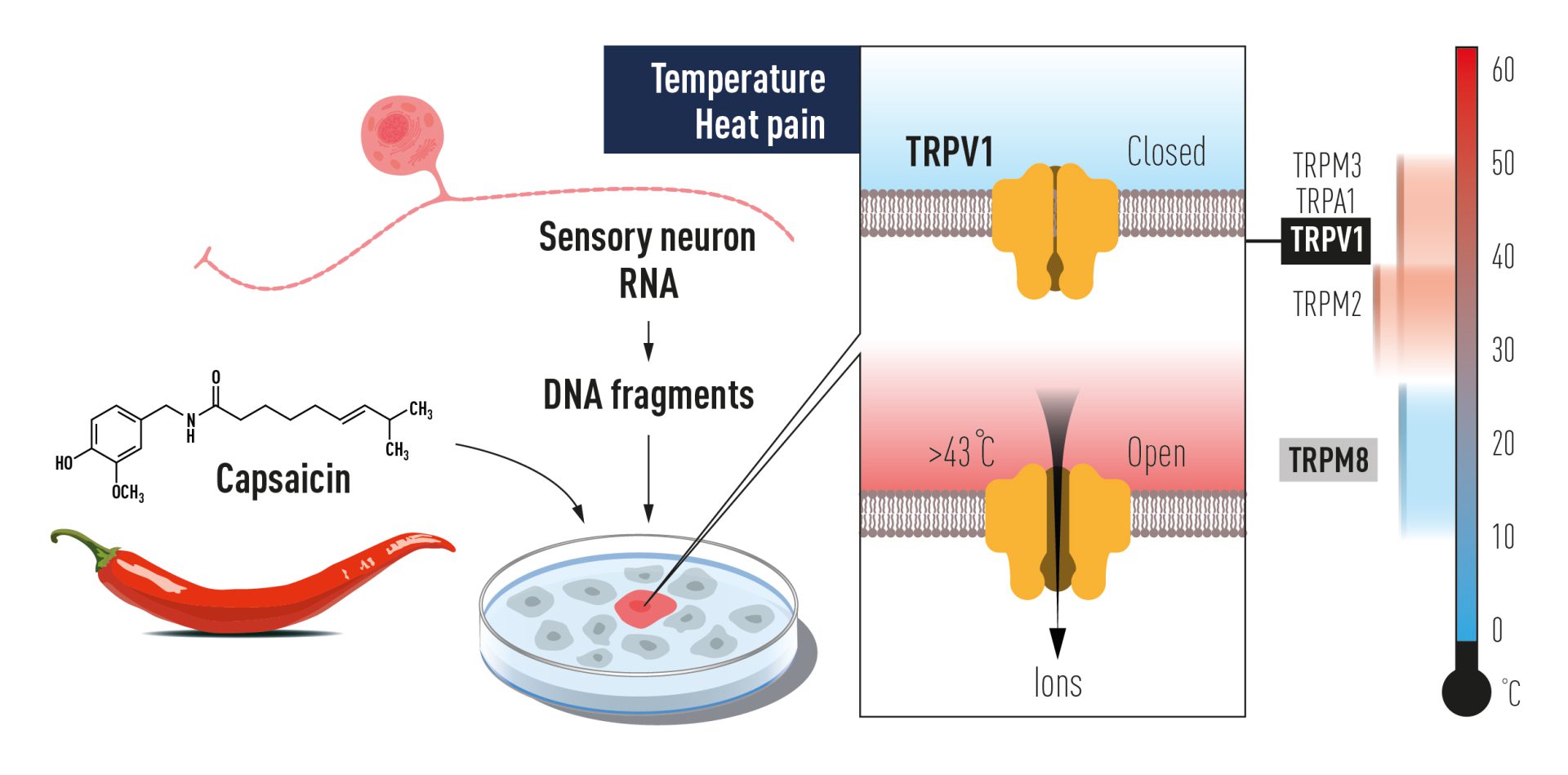
شکل ۲ دیوید جولیوس از کپسایسین تهیهشده از فلفل قرمز برای شناسایی TRPV1، یک کانال یونی که با حرارت دردناک فعال میشود، استفاده کرد. کانالهای یونی مرتبط دیگر شناسایی شد و اکنون میفهمیم که چگونه دماهای مختلف میتوانند سیگنالهای الکتریکی را در سیستم عصبی القا کنند
کشف ژن TRPV1 پیشرفت بزرگی بود که راه را برای کشف گیرندههای اضافی حسگر دما پیش برد. فارغ از یکدیگر، دیوید جولیوس و اردم پاتاپوتیان از ماده شیمیایی منتول برای شناسایی ژن TRPM8 استفاده کردند که در بازوی بلند کروموزوم شماره 2 بهصورت 2q37.1 مستقر است. این ژن گیرندهای است که در اثر سرما فعال میشود. کانالهای یون اضافی مربوط به TRPV1 و TRPM8 شناسایی و مشخص شده است که با طیف وسیعی از دماهای مختلف فعال میشوند. بسیاری از آزمایشگاهها با استفاده از موشهای دستکاریشده ژنتیکی که فاقد این ژنهای تازه کشف شده بودند، نقشهای این کانالها را در احساس حرارتی بررسی کردند. کشف دیوید جولیوس از TRPV1 پیشرفت بزرگی بود که به ما اجازه داد بفهمیم تفاوت دما چگونه میتواند سیگنالهای الکتریکی را در سیستم عصبی ایجاد کند.
در حالی که مکانیسمهای احساس دما در حال شکلگیری بود، اما هنوز مشخص نبود که چگونه محرکهای مکانیکی را میتوان به حس لامسه و فشار تبدیل کرد. محققان قبلاً حسگرهای مکانیکی را در باکتریها پیدا کرده بودند، اما مکانیسمهای زیربنایی لمس در مهرهداران ناشناخته بود. اردم پاتاپوتیان که در Scripps Research در لاجولا، کالیفرنیا، ایالات متحده کار میکرد، مایل بود گیرندههای گریزی را که توسط محرکهای مکانیکی فعال میشوند، شناسایی کند.
پاتاپوتیان و همکارانش ابتدا یک ردیف سلولی را شناسایی کردند که هنگامی که تکتک سلولها با میکروپیپت زده میشدند، یک سیگنال الکتریکی قابل اندازهگیری میداد. فرض بر این بود که گیرنده فعالشده توسط نیروی مکانیکی، یک کانال یونی است و در مرحله بعدی 72 ژن نامزد کُدکننده گیرندههای احتمالی شناسایی شدند. این ژنها یکییکی غیرفعال شدند تا ژن مسئول حساسیت مکانیکی در سلولهای مورد مطالعه کشف شود. پس از جستجوی سخت، پاتاپوتیان و همکارانش موفق به شناسایی یک ژن واحد شدند که خاموش شدن آن باعث میشد سلولها نسبت به فشار دادن میکروپیپت حساس نباشند. یک کانال یون کاملاً ناشناخته مکانیکی جدید کشف شد و نام Piezo1، از کلمه یونانی برای فشار (í؛ píesi) نامگذاری شد. از طریق شباهت آن به Piezo1، ژن دوم کشف شد و Piezo2 نام گرفت. مشخص شد که نورونهای حسی، سطوح بالای Piezo2 را بیان میکنند و مطالعات بیشتر ثابت کرد که Piezo1 و Piezo2 کانالهای یونی هستند که مستقیماً با اعمال فشار بر غشای سلولی فعال میشوند (شکل 3).
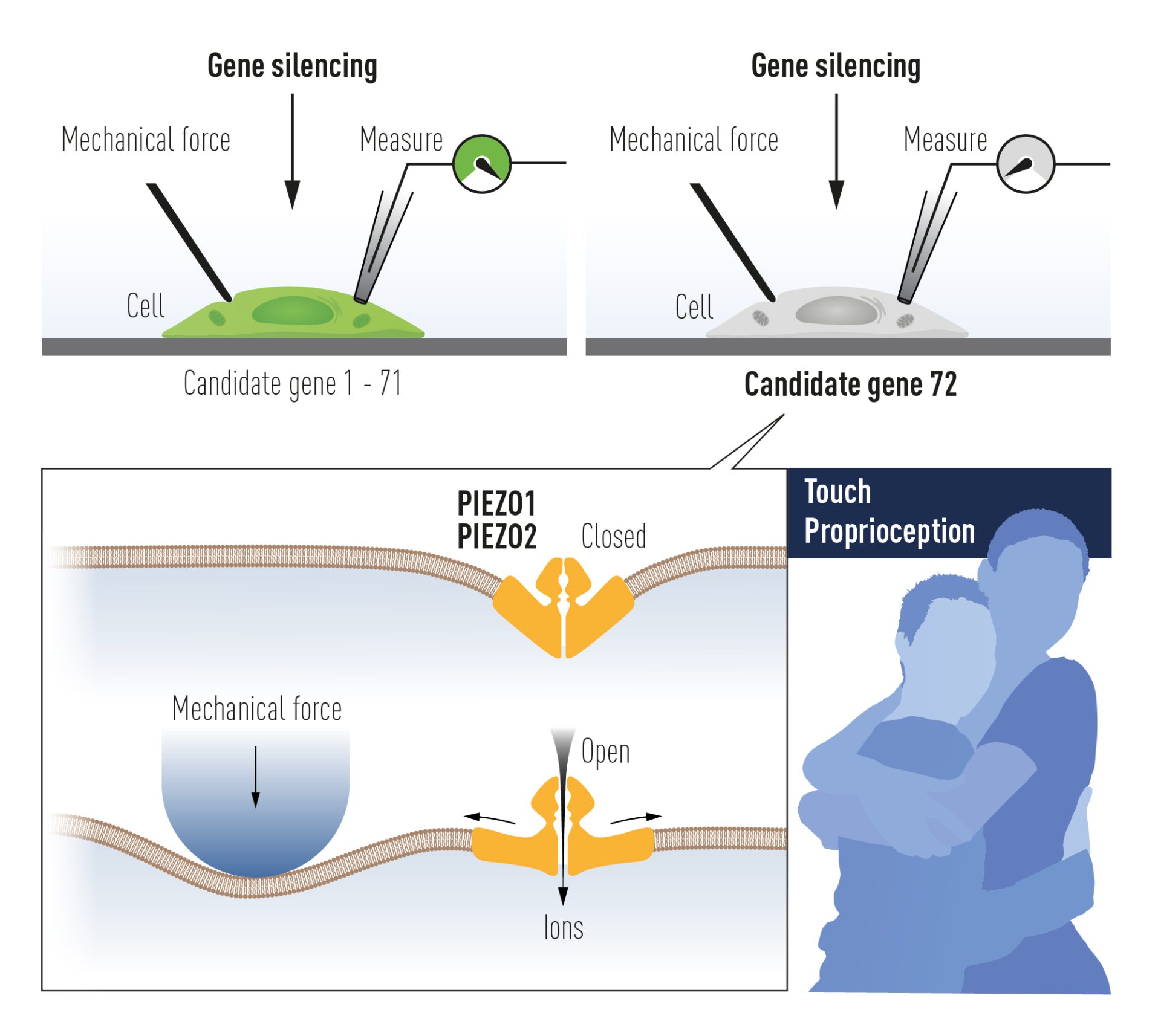
شکل ۳ شماتیکی از مسیر مولکولی خاموش شدن ژنهای کاندید در حس لامسه و فشار مکانیکی و مکانیسم عملکرد کانالهای یونی PIEZO1 و PIEZO2
دستیابی به موفقیت توسط پاتاپوتیان منجر به مجموعهای از مقالات از وی و گروههای دیگر شد که نشان میداد کانال یونی Piezo2 برای حس لامسه ضروری است. علاوه بر این، نشان داده شد که Piezo2 نقش مهمی در حساسیت بسیار مهم موقعیت و حرکت بدن دارد که به عنوان حس عمقی شناخته میشود. در کارهای بعدی، مشخص گردید که کانالهای Piezo1 و Piezo2 فرآیندهای فیزیولوژیکی مهم دیگری از جمله فشارخون، تنفس و کنترل مثانه را تنظیم میکنند.
اکتشافات پیشگامانه کانالهای TRPV1، TRPM8 و Piezo توسط برندگان امسال جایزه نوبل پزشکی به ما این امکان را داده است که بفهمیم چگونه گرما، سرما و نیروی مکانیکی میتوانند تکانههای عصبی را ایجاد کنند که به ما امکان درک و سازگاری با دنیای اطراف را میدهد. کانالهای TRP برای توانایی ما در درک دما بسیار مهم هستند. کانال Piezo2 به ما حس لامسه و توانایی احساس موقعیت و حرکت اعضای بدن را میبخشد. کانالهای TRP و Piezo همچنین به عملکردهای فیزیولوژیکی اضافی متعددی کمک میکنند که به حس دما یا محرکهای مکانیکی بستگی دارد. تحقیقات فشرده در حال انجام و منبعث از جایزه نوبل پزشکی امسال به اکتشافات جدیدی میپردازد و بر روشن ساختن عملکرد آنها در انواع فرآیندهای فیزیولوژیکی متمرکز است. این دانش برای توسعه درمان طیف گستردهای از بیماریها، از جمله بیماری درد مزمن استفاده میشود (شکل 4).
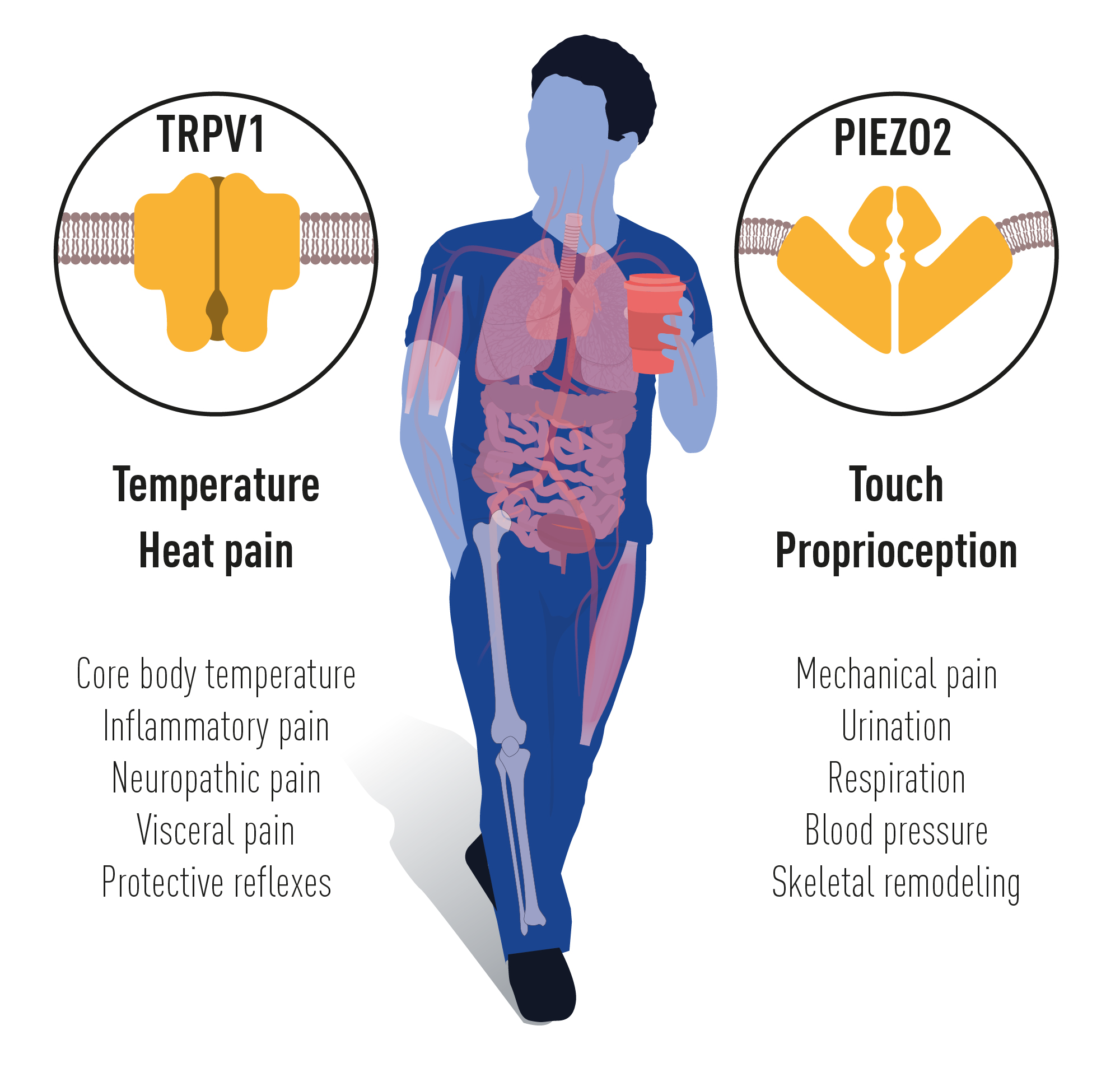
شکل ۴ کشفیات مهم برندگان امسال جایزه نوبل توضیح داده است که چگونه گرما، سرما و لمس میتوانند سیگنالهایی را در سیستم عصبی ما ایجاد کنند. کانالهای یونی شناسایی شده برای بسیاری از فرآیندهای فیزیولوژیکی و شرایط بیماری مهم هستند.
- - نشانی ایمیل شما منتشر نخواهد شد.
- - لطفا دیدگاهتان تا حد امکان مربوط به مطلب باشد.
- - لطفا فارسی بنویسید.
- - میخواهید عکس خودتان کنار نظرتان باشد؟ به gravatar.com بروید و عکستان را اضافه کنید.
- - نظرات شما بعد از تایید مدیریت منتشر خواهد شد

